This post is also available in: English 简体中文
本周二,輝瑞公司向美國FDA提出申請,要求批準為5歲以下兒童提供超低劑量的COVID-19疫苗,5歲以下兒童有可能從3月初開始就可以接種疫苗。
在整個過程中,美國FDA曾敦促輝瑞公司及其合作夥伴BioNTech公司,希望他們能盡早提出申請。
美國1900萬5歲以下的兒童是唯一沒有資格接種冠狀病毒疫苗的群體。許多家長一直在推動將疫苗接種範圍擴大到幼兒和學齡前兒童。特別是在Omicron疫情期間,創紀錄的青少年感染者開始住院。
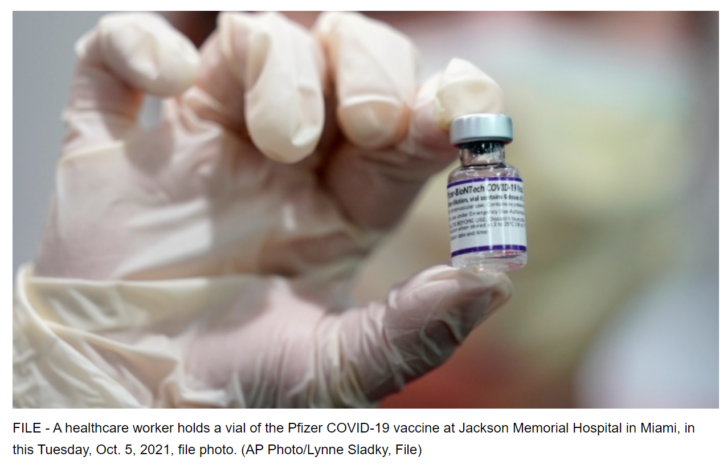
如果FDA同意,輝瑞公司的兒童疫苗劑量僅為成人的十分之一,就可以給6個月大的嬰兒註射。
一個有待解決的問題是兒童需要打多少針。輝瑞公司正在測試第三劑,因為兩劑接種對於嬰兒來說已經足夠,但對學齡前兒童來說可能還不夠,而研究的最終數據預計要到3月下旬才能出來。
這意味著美國FDA可能會考慮暫時批準兩針,如果研究結果支持的話,第三針可能會被追加批準。
該機構的決定可能在幾周內作出,但這並不是唯一的障礙。
拜登政府一直試圖加快授權為兒童註射COVID-19疫苗,認為疫苗接種對於學校和日間護理中心的開放,以及讓父母不再擔心小孩,能夠回去工作至關重要。
然而,兒童的疫苗接種率一直低於其他年齡組。根據美國兒科學會的數據,截至上周,只有20%的5至11歲兒童,12至17歲接種疫苗的兒童也剛過一半,然後成年人已經有4分之三已完全接種疫苗。
雖然幼兒感染病毒後轉重癥的可能性遠低於成人,但這種情況也可能發生,而且目前兒童COVID-19的感染率比疫情中的任何時候都高。
科羅拉多大學的Sean O’Leary說:”我們現在看到的是這個年齡段仍然有很多人住院,不幸的是還有一些人死亡。如果美國FDA批準為這些青少年接種疫苗,這將是非常重要的,因為所有這些住院和死亡基本上是可以預防的。”
對於5歲以下的孩子,輝瑞公司的實驗是給參與者打兩針,間隔三周,然後至少兩個月後再打第三針。
12月,輝瑞公司宣布,從實驗數據來看2歲以下的兒童得到了疫苗保護,但2至4歲兒童的抗體反應太低。目前還不清楚原因,但一種可能性是超低劑量對學齡前兒童來說有點太低。
由於初步結果顯示註射是安全的,輝瑞公司在測試中增加第三劑量,希望能改善保護。
文章來源: CP24
作者: Lauran Neergaard And Matthew Perrone, The Associated Press
中文:加國無憂

